传统金属支架植入冠脉后,确实会带来一些不可逆的影响,比如血管舒缩受限、长期异物刺激等,当然更会阻碍血运重建。因此,我们盼望支架能够“事了拂衣去,深藏身与名”,于是生物可降解支架应运而生。
可降解支架简史
42年前,当Grüntzig等用单纯球囊扩张进行世界上第一次PCI时,可能对单纯球囊扩张后的再狭窄并没有什么概念。为了对扩张后的血管进行支撑、降低再狭窄率,33年前我们又发明了支架。
至于可降解支架的出现,实际上也并不是很晚,目前为止大约有21年的历史。虽然出现得早,研究也做了不少,但目前可降解支架在冠心病中的应用仍然受到严格限制,正如2018年ESC心肌血运重建指南中所提到的,可降解支架目前为止仅能用于科学研究目的。
最早的可降解支架是日本研发的Igaki–Tamai,是一款聚合乳酸制成的无药物涂层支架。2012年Circulation上报道了植入Igaki–Tamai的50名患者10年随访结果,血管内超声(IVUS)发现,绝大多数支架都在3年内消失,而1年、5年、10年的靶血管血运重建率分别为16%、18%、28%,让当时的众人看到了一点希望。
随后入场的是目前可降解支架领域最重要的玩家——Absorb,同样由聚合乳酸制成以保证可吸收,与享誉盛名的CoCr-EES支架(钴络合金支架梁+依维莫司涂层,代表作为Xience)一样使用依维莫司涂层以减少再狭窄。2010年,根据ABSORB研究的结果,获得了欧洲的CE认证;而更为谨慎的美国FDA,则在2015年ABSORB III研究结果出炉后批准其在美国使用。
2015年发表在NEJM上的ABSORB III研究将2008名患者按照2:1的比例分入Absorb组或“金标准”CoCr-EES组,随访1年内的靶病变失败率在Absorb组为7.8%,在CoCr-EES组为6.1%。尽管存在小小差异,但却达到了最初设计的非劣效终点。
然而,晴朗的天空随后却出现了一片又一片阴云。2016年Lancet上的一篇荟萃分析汇总了此前3738名患者的1年随访结果,认为Absorb可能会增加支架内血栓风险近1倍,尤其在植入最初30天内,风险更是增加了2.11倍。同样在2016年Lancet上发表ABSORB II的3年随访结果则发现,Absorb组的复合终点(心脏死亡、靶血管心梗与靶血管血运重建)为CoCr-EES组的2.17倍。
2017年发表在NEJM上的AIDA研究成为了压倒骆驼的最后一根稻草。该研究共1845名患者随机植入Absorb支架或CoCr-EES支架,在随访2年时尽管靶血管失败率没有出现显著差异,但Absorb组的支架内血栓风险为3.5%,远大于CoCr-EES组的0.9%。随后,就在2017年,Absorb被撤出市场。
由于Absorb存在自身缺陷(比如支架梁厚度、降解速度、机械强度等),目前尚不能得出可降解支架没有前景的结论。近几年我国自己的可降解支架研发热情也非常高涨,目前为止取得了不错的成果,代表作品有华安的Xinsorb、乐普的NeoVas、微创的Firesorb、先健的IBS、阿迈特的AMsorb等,我们会在最后进行介绍。
要想了解可降解支架,还是要从Absorb开始。
1. Absorb
Absorb支架使用了最常用于可降解支架的聚合乳酸,现在也有以镁或铁为基础的可降解支架。聚合乳酸植入后会降解为乳酸单体,最终代谢为CO2和水,实现“可降解”。
相比于金属,聚合乳酸最大的问题在于机械强度不足,因此支架梁不得不变得更厚,尽管如此,其强度也只能达到金属支架的一半。支架覆盖血管壁面积从CoCr-EES的13%变为了Absorb的27%,阻碍了内皮覆盖支架梁,为之后出现不良事件埋下伏笔。
在进入临床试验前,Absorb在猪、兔等动物上进行了一些动物试验。
一项研究评估了猪冠脉内263枚Absorb与72枚CoCr-EES,发现不同时间点造影与IVUS显示的最小管腔面积在两种支架之间并不相同。在植入的6个月内,Absorb的管腔缩小比CoCr-EES更为严重;然而在12-42个月时,植入Absorb的血管管腔逐渐增大,而CoCr-EES组没有发现管腔增大。这种变化可能由于支架降解后不再影响血管重塑,因而随着实验动物长大而管腔增大,但金属支架则不具备这种优点。
组织学观察发现,1个月与6个月时,Absorb的狭窄确实较严重,但在30个月、36个月与42个月时则反转过来,Absorb的狭窄更轻。在植入1个月后,所有支架都被内膜完整覆盖,不过两种支架周围都出现了纤维蛋白。Absorb的炎症积分在6、12、18个月都明显更高,12个月时更是达到顶峰。随后,尽管炎症积分下降,但在30、36、42个月时仍显著比CoCr-EES高。在1个月与3个月时,仅有0.7%的Absorb发生断裂,但和既往相同时间点的micro-CT扫描结果相比显得有些低估。扫描电镜发现尽管两种支架的厚度不同,但在1个月时Absorb与CoCr-EES都能完全内皮化。不过在另一项使用兔子的研究中,Absorb在28天时的内皮覆盖率要低一些。所以在不同的动物模型中,内皮化存在不小的差异,很难推测人类冠脉的内皮化情况。
Ormiston等则在体外动脉研究中发现,在主支动脉球囊扩张中(球囊直径5.5 mm,压力22 atm),3.0 mm Absorb不发生断裂的后扩张阈值为20 atm & 3.8 mm;在3.0 mm非顺应性边支球囊扩张中,Absorb断裂阈值为10 atm;而对于Multi-Link型支架,22 atm无论主支还是边支均不会发生断裂。非顺应性球囊的Mini-kissing后扩张在3.0 mm的Absorb中安全阈值为5 atm,但即使20 atm时Multi-Link型支架也不会断裂。另外一项暂未发表的动物研究中,micro-CT显示1、3、6个月时Absorb断裂率逐渐增加,同时也发现钙化明显增加(尤其在靠近管腔处),推测可能聚合乳酸降解促进了钙化。
内皮化过程中,血流剪切非常重要,低内皮剪切力会影响内皮化速度。无论支架梁厚度如何,非流线形的支架梁都会降低剪切力,从而内皮化速度减慢;同时,纤维蛋白原、炎症细胞的滞留时间增加,共同导致血栓风险增加。同样的道理,增厚的支架梁也会增加血栓风险。
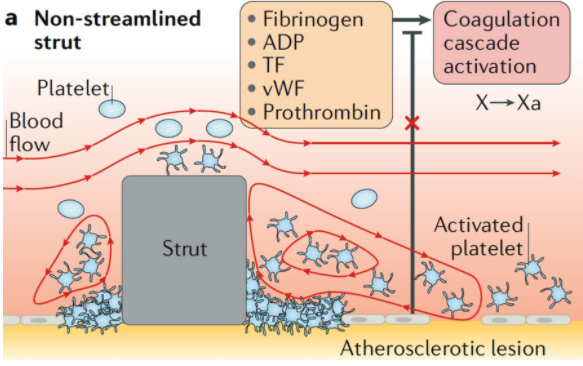
图1 厚支架梁增加血栓风险
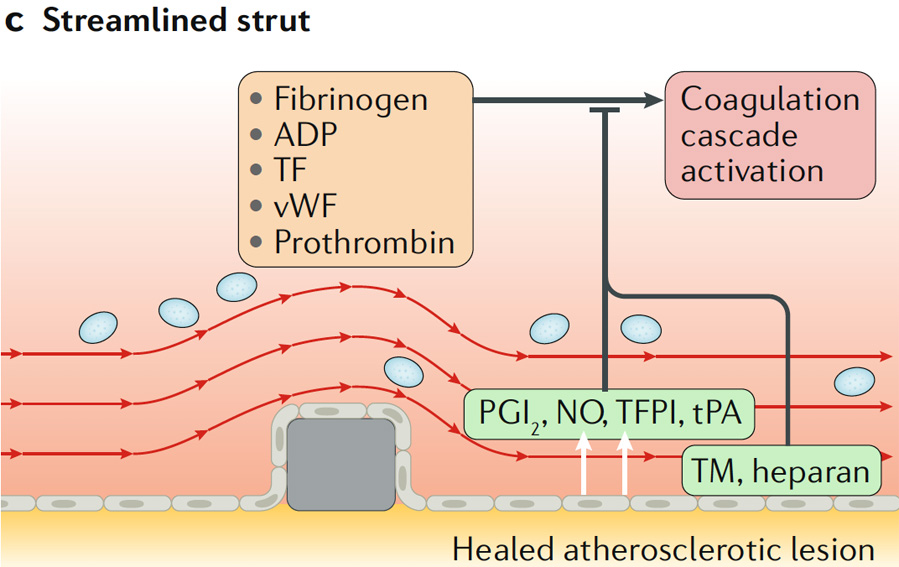
图2 薄支架梁降低血栓风险
在既往的动物实验中发现,支架梁厚度>100 μm时血栓风险明显高于支架梁厚度<100 μm。Simon等在体外证实支架梁厚度会影响内皮细胞覆盖与迁移,分界点为75 μm。不过我们也要注意,人类的内皮化速度要明显慢于这些实验动物,因为实验动物往往更年轻,动脉更健康,而冠心病患者年纪更大,血管条件也更差。
在猪实验中,Absorb厚支架梁导致的血栓形成风险明显高于目前市面上能见到的几种薄支架梁支架。在兔实验中,Absorb的内皮化速度明显比药物洗脱支架或裸金属支架慢。除支架梁厚度外,Absorb覆盖的血管壁面积大(27%,对比Multi-Link型支架的13%),同样会阻碍内皮化过程。
目前,大规模、多中心的几项临床研究显示,Absorb与CoCr-EES在1年时壯陽藥 心脏性死亡或靶病变血运重建风险相似,但支架内血栓风险更高,大约为1.3% vs. 0.5%。大型荟萃分析显示,无论是早期(<30天)、晚期(30天-1年)还是极晚期(>1年)支架内血栓,Absorb都比CoCr-EES更高;同时,缺血驱动的靶病变血运重建在Absorb组也更高,但两组的心脏性死亡风险相同。
在2018年,上面提到的AIDA研究又公布了全部的2年随访结果,显示靶血管失败复合终点(心脏性死亡+心肌梗死+靶血管血运重建)在Absorb组为11.0%,而CoCr-EES组为9.9%,虽然符合开始定下的非劣标准,但支架内血栓风险仍然为3.76倍。ABSORB II公布的3-4年间随访结果发现,事件风险会逐渐衰减,Absorb组的靶血管失败复合终点由10.5%增加到了11.5%,CoCr-EES组则从5.0%增加至6.0%,在此期间两组都没有发生支架内血栓。
我们必须思考一个问题:什么因素才是支架内血栓形成最重要的?(推荐阅读:成功PCI术后却死亡,冠脉介入后最严重的并发症了解一下)支架内血栓通常与植入过程最为相关,比如支架直径选择不当、支架贴壁不良、支架膨胀不全等,而与支架本身的关系较小。目前提倡的PSP——良好预扩张(optimal Pre-dilatation)、恰当选择支架尺寸(vessel and device Sizing)、后扩张(Post-dilatation)——可以显著减少支架内血栓风险。既往的RCT研究与队列研究显示,平均后扩张率竟然低于50%,可想而知,冠脉内成像(IVUS与OCT)比例就更低了。
将既往的ABSORB系列研究汇总后发现,Absorb支架植入时的最佳预扩张、恰当选择尺寸与后扩张的比例分别只有可怜的59.2%、81.6%和12.4%,这三个重要步骤均能独立降低靶血管失败与支架内血栓风险。而在AIDA研究中,尽管预扩张(97%)与后扩张(74%)的比例已经很高了,但支架内血栓仍然在Absorb组中较高。因此,手术技巧对于Absorb支架内血栓的影响仍不能确定。
除Absorb外,截止到2018年4月,还有另外4种可降解支架获得了欧盟的CE许可,分别是ART-BRS、DESolve、Fantom与Magmaris。
2. ART-BRS
ART-BRS使用了不同于Absorb的聚合乳酸(Absorb全为L-乳酸,而ART-BRS中加入了2%的D-乳酸),支架梁厚度为170 μm,不过支架梁覆盖血管面积<25%,与金属裸支架相似地未使用药物涂层。相比其他可降解支架,ART-BRS的降解更加迅速,从植入3个月就开始降解,到6个月时仅剩下植入时的10%,24个月时完全检测不到。
在植入猪冠脉的36个月随访中,ART-BRS在1个月内迅速内皮化,与裸金属支架相似。1个月时狭窄程度明显比裸金属支架更重,不过从3个月开始观察到管腔逐渐扩大,9个月时的管腔明显较1个月时大,这种扩大可以延续到24个月。管腔扩大伴随的是炎症积分更高,3个月时达峰,12个月时仍比较高。随后尽管炎症下降,但ART-BRS的炎症在24个月内都比裸金属支架高。
ARTDIVA研究是ART-BRS的首个临床研究,纳入了30名患者,在6个月时无一人出现心脏性死亡、心肌梗死或靶血管血运重建。至今为止,还没有其他相关临床研究,因此,ART-BRS也没有商业化生产。
3. DESolve
DESolve使用了与Absorb相同的材质,支架梁厚度为150 μm,3.0 mm的支架血管壁覆盖面积为30%,使用类似于雷帕霉素的novolimus作为抗增殖药物。DESolve在两端各有一个铂做的标记,协助在X线透视下植入。支架的novolimus含量为3 μg/mm,>85%的药物在4周内释放。DESolve使用了专属的喷涂技术,省去了不必要的底部涂层,保证了涂层厚度<3 μm。
DESolve与Absorb的差异在于弹性,DESolve可以扩大到更大的直径,断裂风险却很小,同时本身的设计可以尽量避免微小的贴壁不良。Ormiston等发现3.0 mm的DESolve在20 atm、后扩张球囊5 mm时仍不会断裂。
DESolve的动物实验结果很少。2014年的一项研究使用OCT观察植入后的DESolve,发现支架在2年内吸收完全,1年时吸收>95%。37℃的体外研究显示,支架可以保持完整、给予径向支撑≥3个月。DESolve与Multi-Link型支架在部署后1分钟均会回缩约0.1 mm,在1-10分钟时均没有变化,而10-60分钟时DESolve会扩大,Multi-Link型支架不会变化,这种特性可能对支架贴壁有好处,但可能并不会提供多少支撑力,因为DESolve的径向强度比Absorb还差,更不用说与Multi-Link型支架相比了。
2014年的DESolve FIM研究纳入了16名患者,6个月时QCA下的晚期管腔损失为0.19±0.19 mm,OCT下的新生内膜为0.12±0.04 mm。
DESolve Nx研究纳入了122名稳定型心绞痛的患者,6个月时的晚期管腔损失为0.20±0.32 mm。在这项研究中,2年时确定的支架内血栓、心脏性死亡与临床驱动的靶血管血运重建分别为0%、2.5%与4.1%,不过在第1个月时观察到了1例可能的支架内血栓。DESolve Nx研究5年随访的初步数据中仍未发现确定的支架内血栓,心脏性死亡与临床驱动的靶血管血运重建较2年时也没有变化。2018年的多中心上市后研究纳入了100名患者、109个病变,1年时无心脏性死亡,1%发生确定支架内血栓,1%发生心梗,3%接受靶血管血运重建。
DESolve Cx是新一代的DESolve支架,支架梁厚度仅为120 μm。初步的临床研究数据显示,在1年内未发生确定支架内血栓、心脏性死亡、临床驱动的靶血管血运重建或靶血管心肌梗死。2014年,DESolve支架梁厚度100 μm的版本被批准用于临床,对血流的影响更小。不过Boeder等报道,管腔最小面积在100 μm版本中相比150 μm版本更小,植入后残余狭窄更多,提示100 μm的径向支撑力堪忧。
4. Fantom
Fantom是使用PTD-PC材料制成的不透射线支架,支架梁厚度为125 μm,使用雷帕霉素涂层(115 μg在3.0×18.0 mm的支架上)。与其他可降解支架相比,它最大的特点是在支架材质中加入了碘,方便在X线下观察支架降解情况。
尽管支架梁只有125 μm,但支架弹性与径向支撑还算不错,后扩张可以有0.75-1.00 mm的超过余地。动物实验发现,在12个月时血管舒缩功能可以恢复。支架的吸收时间大约36个月,与绝大多数聚合乳酸支架相同,>80%的支架体消失于第1年内。
FANTOM II cohort A研究在6个月时评估了117名在de novo病变中植入Fantom的患者,晚期管腔损失为0.25±0.40 mm。随访期间未发生心脏性死亡,0.9%的患者出现支架内血栓,2.6%的患者出现MACE事件(2例心梗,2例靶血管血运重建)。FANTOM II cohort A和cohort B研究的初步数据中包括240名患者,2年随访期间心脏性死亡、心肌梗死、临床驱动的靶血管血运重建分别为0.8%、1.7%、2.9%,共出现1例早期支架内血栓、1例极晚期支架内血栓。
5. Magmaris
目前的Magmaris使用慢降解的镁合金制成,支架梁厚度为150 μm,雷帕霉素含量为140 μg/cm²。镁合金可以透过X线,因此在两侧使用钽作为marker来增强可视性。
第一代可降解金属支架(AMS-1)使用93%镁、7%稀土元素的合金,在没有药物涂层的情况下厚度为165 μm。AMS-1与不锈钢支架相似,弹性回缩非常少(<8%),可耐受压力较高,缩短很不明显。在植入60天后,AMS-1变为离子从而降解。早期的临床试验发现晚期管腔损失太严重(1.08±0.49 mm),可能与降解太快导致的失去支撑、血管回缩相关。
AMS-1后来被重新设计为DREAMS 1 G,增加了紫杉醇涂层(7.4 μg/cm²),并且在镁合金表面使用聚合乳酸包被用来减慢降解速度。这个版本在46名患者中进行测试,3年时的靶血管失败率为6.6%,没有发生心脏性死亡或支架内血栓。
最新版本被命名为Magmaris(此前也被称作DREAMS 2 G),使用了方形支架梁与侧面电解抛光来降低降解速度、预防断裂。与其他金属支架一样,镁可以提供较好的强度,较低的弹性回缩,对血管形状有更好的顺应性。电解抛光也为支架提供了更柔和的边缘,使得支架更好输送,对支架梁周围的血流动力学也有好处。
支架的降解分为两个主要步骤:氧化反应+转化为磷酸钙。在第一步中,镁合金在水中氧化,变为氢氧化镁;随后的第二步中氢氧化镁转化为磷酸镁,最后变成磷酸钙。
尽管两种支架的支架梁厚度相同,但有报道在动物实验中,Magmaris的内皮化速度较Absorb更快。在植入猪体内3天后,Magmaris支架梁内皮化达到了47.0±4.1%,而Absorb只有31.4±9.2%。而在植入兔体内28天后,Magmaris支架梁内皮化达73.8±10.5%,Absorb只有59.2±8.0%。Magmaris用OCT评估狭窄发现最严重时是3个月,随后逐渐减轻直到2年,在此期间与CoCr-EES的差别不大,在实验中未发现Magmaris组的血管增大。Magmaris的药物释放速度与降解速度较慢,在90天时释放了69.4%的雷帕霉素,1年时降解支架的98.4%。还有研究认为,Magmaris的血小板粘附、聚集也较Absorb轻。
2016年的BIOSOLVE II研究在123名患者中测试了Magmaris,6个月时QCA的晚期管腔损失为0.44±0.36 mm,没有发生支架内血栓事件。出现了4例靶病变失败,其中1例为心脏性死亡,1例为围术期心梗,2例缺血驱动的靶血管血运重建。在这项研究中6-12个月的QCA结果相对稳定,也未再发生临床事件。2年时靶病变失败率为5.9%,其中2例为心脏性死亡,1例为靶血管心梗,4例为靶血管血运重建,未发生支架内血栓事件。3年随访的初步报告显示靶病变失败率为6.8%,也还是未发现支架内血栓。BIOSOLVE IV纳入了200名患者植入Magmaris,12个月时靶病变失败率为4.6%,支架内血栓出现1例。
DREAM 3 G目前尚在研发中,支架梁更薄(99-150 μm),与Magmaris相似的1年内降解。
尽管有些结果看上去很美好,但对这些非随机对照的小型临床试验结果解释需谨慎。君不见Absorb的初期试验也很美好,但并不能转化到ABSORB III这些大型临床研究中来。
可降解支架与支架内血栓
其实早在ABSORB系列大型临床研究结果揭示前,专家们就已经开始顾虑可降解支架的支架内血栓问题。2015年Bern大学报道了4例支架内血栓,分别发生在Absorb支架植入后的19、19、21、44个月,其中有3例与支架贴壁不良、支架梁暴露有关,可以观察到血栓与支架直接接触,有2例更是支架梁跑到了管腔中央。这种贴壁不良与既往金属支架时代的贴壁不良不同,因为很可能是支架部分降解导致的支架断裂。即使在动物实验中,Absorb的完全吸收也需要36-42个月,而人类往往更久。
Sotomi等分析了43例支架内血栓的的冠脉内影像,其中17例为急性或亚急性,26例为晚期或极晚期。急性或亚急性支架内血栓最常见的原因是贴壁不良(23.5%),随后是支架梁未覆盖(17.6%)、支架扩张不足(11.8%)、急性支架断裂(5.9%)、支架重叠(5.9%)与急性支架回缩(5.9%)。而在晚期或极晚期,贴壁不良仍然为最常见的原因(34.6%),随后是晚期支架断裂(30.8%)、支架梁周低密度区域(19.2%)、支架梁未覆盖或支架扩张不足(15.4%)、支架回缩(11.5%)、再狭窄(7.7%)、新生粥样硬化(3.8%)和分叉病变(3.8%)。
Yamaji等评估了36名患者中38个极晚期支架内血栓,中位出现时间为20个月,在42.1%的病变中发生支架断裂,其他原因为贴壁不良(18.4%)、新生动脉粥样硬化(18.4%)、支架扩张不全或回缩(10.5%)、支架梁覆盖不全(5.3%)与支架边缘病变进展(2.6%)。
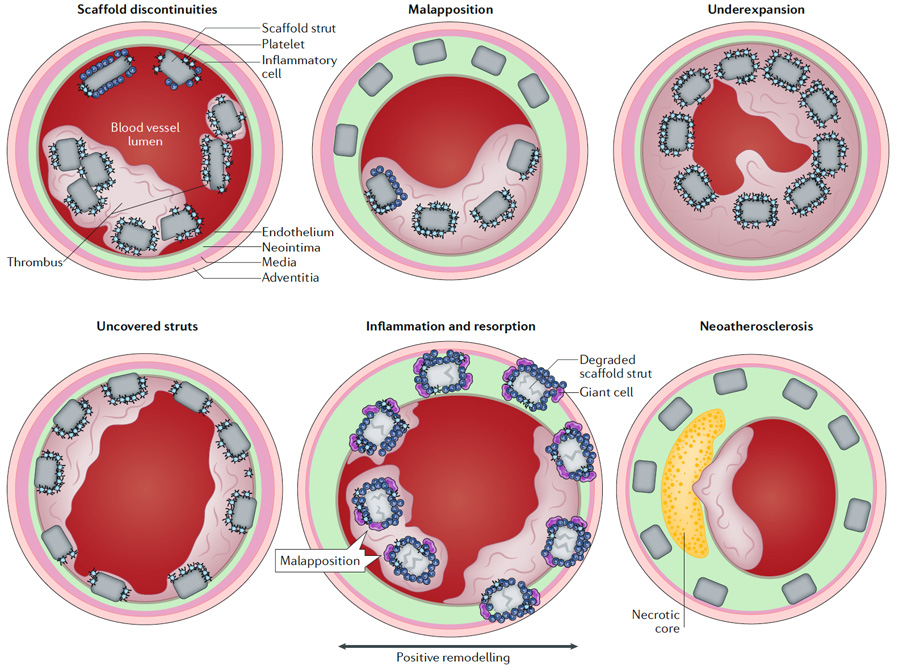
图3 从左上至右下分别为断裂、贴壁不良、扩张不全、支架梁覆盖不全、炎症、新生粥样硬化
1. 支架断裂
支架断裂有不同的定义,应用最广泛的定义为:无法用支架环形结构解释的至少一个横截面内的孤立支架梁贴壁不良,或连续画面中突然出现的纵向支架梁消失。OCT对于支架断裂的敏感性比较有限。
在ABSORB cohort B临床研究中,支架断裂随着时间而增加,2年时为25%,3年时为42%。支架断裂主要原因是支架梁降解,当然与聚合乳酸脆弱的径向支撑力也有关系。动物实验中曾使用micro-CT评估支架断裂,发现90天时50%的支架发生断裂,而180天时所有支架都发生断裂,平均每个支架断裂10处,同时支架断裂比降解更快,因为只需要降解关键部分就可以导致断裂。
在临床试验中,OCT检查发现的支架断裂则少得多,很可能由于OCT对支架断裂的辨识效果不好。
2. 支架贴壁不良
贴壁不良被定义为支架梁与血管壁之间的缝隙大于支架梁厚度。因为Absorb的支架梁比较厚,更不容易被定义为贴壁不良,但一旦发生贴壁不良对血流的影响也更严重。
Foin等评估了6个月时贴壁不良程度对支架梁覆盖速度的影响后发现,贴壁不良<100 μm的支架梁全部被覆盖,100-300 μm时仅6.1%的支架梁被覆盖,300-500 μm时13.7%的支架梁被覆盖,证明贴壁不良程度与支架梁覆盖速度有关。同时,支架贴壁不良越严重,对血流的影响越大,也就更容易产生血栓。
Iannaccone等一项纳入13个OCT研究的荟萃分析发现,6-12个月的随访期间Absorb的支架贴壁不良风险是所有支架中最高的(3.8%)。
3. 支架梁未被覆盖
支架梁的覆盖速度受很多因素影响,比如支架梁厚度、支架梁材质、抗增殖药物种类与剂量、损伤程度及潜在的粥样硬化状态。Absorb支架梁厚度约为CoCr-EES的2倍,支架梁覆盖不好当然容易产生血栓。
在ABSORB-STEMI TROFI II OCT研究中,95名患者植入了Absorb,另96名患者植入了CoCr-EES,6个月时OCT评估的支架覆盖程度在两种支架中相似,均在99%以上,而愈合分数反而偏向于Absorb。但需要注意,OCT将新生内膜与血栓或纤维蛋白区分开存在一定困难,很可能会将未覆盖的支架梁错判,因此这项研究的结果也造成了不少争议。在兔实验中,确实观察到了Absorb会使支架梁覆盖延迟。
4. 炎症
组织学上观察到Absorb的炎症12个时达峰,随后在血管重塑期间炎症积分一直比CoCr-EES高。我们对Absorb植入人类冠脉后导致的炎症反应知之甚少,仅有少数血栓抽吸与尸检的结果可以参考,发现支架梁周围分布有大量炎症细胞,还有一些纤维蛋白和富血小板血栓。
5. 新生粥样硬化
此前多项研究证实,药物洗脱支架发生支架内新生粥样硬化比金属裸支架更早,而Absorb的情况还不明了。
在Absorb Extend研究中,中位随访67个月时,支架内新生粥样硬化比例为20%。植入1年后载脂巨噬细胞、钙化、新生血管、薄帽纤维斑块的比例分别为17%、28%、6%、0%,5年时的比例分别为61%、94%、78%、22%。
在ABSORB cohort B研究的亚组分析中,33个支架内区域与13个支架外区域在5年时显示出相同的钙化进展程度。
6. 血管舒缩
由于Absorb相关研究提前停止,我们很难观察到支架完全降解后的血管舒缩功能。然而,一些小型研究展示出令人困惑的结果。
血管舒缩功能正常被定义为使用乙酰胆碱或硝酸甘油后血管平均直径变化>4%。在TROFI II研究的3年冠脉评估中(20例Absorb,18例CoCr-EES),60%的患者在使用乙酰胆碱后存在反常血管收缩,Absorb组的比例反而高于CoCr-EES(77.8% vs 25.0%),可能说明覆盖的内皮尚无功能甚至就没有内皮覆盖。硝酸甘油介导的血管舒张一般不依赖于血管内皮,在Absorb组较好,可能证实血管舒缩功能部分恢复。
7. DAPT时长
部分ABSORB系列研究DAPT时长设置为6个月,这种较短的DAPT时长可能与支架内血栓风险升高相关。有时尽管DAPT时长>12个月,只要支架尚未完全降解就仍存在支架内血栓风险,因此有人建议DAPT持续至支架完全降解,但将DAPT延长至3-4年也存在出血风险。
可降解支架的未来在哪里?
目前可降解支架的设计存在较大限制,为了得到较强的支撑力不得不将支架梁增厚,这就导致一系列问题。另外,可降解支架在降解过程中出现的断裂、支架梁暴露、炎症等问题也很棘手。可降解支架的未来在于,是否能将支架梁厚度降下来,是否能找到高强度材料来减少断裂、提供更好的支撑,是否能找到恰当降解时间以恢复血管舒缩功能。
接下来我们简单介绍一下目前出现的下一代可降解支架。
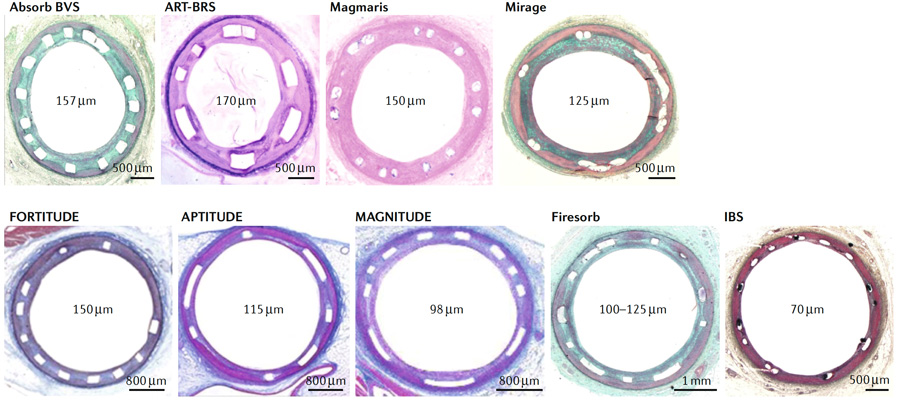
图4 可降解支架的横截面
1. FORTITUDE
FORTITUDE是一款超高分子量聚合乳酸制成的支架,支架梁厚度约150 μm,使用雷帕霉素涂层(101-160 μg,取决于支架大小)。支架在10个月内可完全降解。在第一项临床研究中纳入了68名患者,随访9个月,晚期管腔损失为0.27±0.41 mm,靶血管失败率为4.0%,其中临床驱动的靶病变血运重建1.6%,靶血管心梗3.2%。在9-24个月时,靶血管失败与确定支架内血栓分别为4.9%与1.6%。
这家公司也在开发另外2种下一代可降解支架,APTITUDE与MAGNITUDE,支架梁厚度分别为115 μm与<100 μm。在RENASCENT II研究植入APTITUDE的60名患者初步数据中,9个月随访期间靶血管失败与靶血管心梗均为3.4%,未发生支架内血栓。随后直到24个月未出现新发靶血管失败或支架内血栓。RENASCENT III研究在48名患者中测试了MAGNITUDE,9个月随访期间的靶血管失败与再狭窄分别为6.3%与7.9%,未发生支架内血栓。
2. MeRes100
MeRes100也使用聚合乳酸,雷帕霉素浓度为1.25μg/mm²,使用了新型支架结构并将支架梁厚度限制在100 μm,达到更好的径向支撑力。
在一项临床研究中纳入了108名患者,6个月时QCA的晚期管腔损失为0.15±0.23 mm,OCT中99.3%的支架梁得到覆盖。1名患者在5个月时因非心脏原因死亡,1名患者在6-12个月期间接受了缺血驱动的靶血管血运重建,未报道支架内血栓。在2年随访的初步数据中,缺血驱动的靶血管血运重建为1.87%,未发生支架内血栓。
3. Mirage
Mirage同样使用了聚合乳酸与雷帕霉素涂层,使用了螺旋形结构,可以提供更优秀的弹性。≤3.0 mm版本的支架梁厚度为125 μm,≥3.5 mm版本的支架梁厚度为150 μm。支架的血管壁覆盖面积高达40%-47%。
Mirage在研究中与Absorb进行了对比,60名患者以1:1的比例分配并在30天、6个月、12个月时进行评估,发现晚期管腔损失在两种支架中相同,而12个月时支架内狭窄程度存在显著差异(28.6% vs. 18.2%),靶病变失败率相似,1名在Mirage组的患者出现支架内血栓。
4. XINSORB
XINSORB是葛均波院士支持下我国第一个自主研发的可降解支架,使用160 μm厚的聚合乳酸与雷帕霉素涂层,28天时可以释放80%的药物。第一项临床研究纳入27名患者随访6个月,未发生MACE事件或支架内血栓,晚期管腔损失0.18±0.21 mm。在30个月的初步随访数据中,临床驱动的靶病变血运重建为6.7%,确定支架内血栓为3.3%。
在后来纳入392名患者的临床研究中,200名接受了XINSORB,192名接受了TIVOLI(一种雷帕霉素洗脱金属支架),初步数据显示1年时两组的心脏性死亡、缺血驱动的靶病变血运重建与支架内血栓风险相似。
5. NeoVas
NeoVas使用了聚合乳酸与15.3 μg/mm的雷帕霉素。第一项NeoVas的临床试验纳入了31名患者,6个月时的晚期管腔损失为0.26±0.32 mm,出现1例临床驱动的靶血管血运重建,未发生心脏性死亡或支架内血栓。6个月时OCT发现支架梁覆盖率达95.7%。
随后,1项纳入560人的随机对照研究按照1:1的比例将患者分入NeoVas组或CoCr-EES组。1年时晚期管腔损失在NeoVas组为0.14±0.36 mm,CoCr-EES组为0.11±0.34 mm,OCT下NeoVas的支架梁覆盖率更高(98.7% vs. 96.2%),支架贴壁不良也更少(0.0% vs. 0.6%)。两组在1年时的临床结果相同。
6. Firesorb
Firesorb在2.5 mm的支架中使用100 μm聚合乳酸,3.0 mm使用125 μm,在靠近管腔的表面使用了4 μg/mm的雷帕霉素,支架吸收时间为36个月。
在第一项临床研究——Future-I中纳入了45名患者,2年时1例患者因心梗需要血运重建,未发生心脏性死亡或支架内血栓。
7. IBS
IBS支架梁厚度为53 μm,使用等离子氮激光切割纯铁制造出氮化铁支架,再电镀上锌,最后加上235 μg/cm²的雷帕霉素涂层。由于金属制成,径向支撑力与CoCr-EES类似,3×18 mm IBS的最大扩张直径为4.4 mm。
在植入兔腹主动脉后后,3个月时的降解百分比仅为2.0±1.8%,6个月时为45.9±9%,13个月时为95±4%。动物研究中,28天时支架被完全覆盖,13个月时OCT已无法分辨出支架,而micro-CT显示支架梁已非常小并继续降解。目前临床研究仍在进行中。
8. AMsorb
AMsorb的制作材料同样为聚合乳酸,但使用了独特的3D打印技术制作支架,使支架梁横截面更圆润,同时减少了支架的横截面积(相比Absorb减少了约50%),可能对减少支架内血栓有一定效果。AMsorb在两侧使用了显影marker以协助植入。AMsorb在动物实验中获得了不错的结果,目前临床研究尚在进行中。
参考文献:
[1] Byrne R A, Stone G W, Ormiston J, et al. Coronary balloon angioplasty, stents, and scaffolds[J]. The Lancet, 2017, 390(10096): 781-792.
[2] Jinnouchi H, Torii S, Sakamoto A, et al. Fully bioresorbable vascular scaffolds: lessons learned and future directions[J]. Nature Reviews Cardiology, 2018: 1.